Okrem technológie bola syntéza glykozidov vždy zaujímavá aj pre vedu, pretože ide o veľmi bežnú reakciu v prírode. Nedávne práce Schmidta a Toshimu a Tatsutu, ako aj mnohé v nich uvedené odkazy, sa venujú širokej škále syntetických možností.
Pri syntéze glykozidov sa viaccukrové zložky kombinujú s nukleofilmi, ako sú alkoholy, sacharidy alebo proteíny. Ak je potrebná selektívna reakcia s jednou z hydroxylových skupín sacharidu, všetky ostatné funkcie musia byť v prvom kroku chránené. V princípe môžu enzymatické alebo mikrobiálne procesy vďaka svojej selektivite nahradiť zložité kroky chemickej ochrany a deprotekcie, aby sa selektívne oddelili od glykozidov v určitých oblastiach. Avšak vzhľadom na dlhú históriu alkylglykozidov nebolo použitie enzýmov pri syntéze glykozidov široko študované a aplikované.
Vzhľadom na kapacitu vhodných enzýmových systémov a vysoké výrobné náklady nie je enzymatická syntéza alkylpolyglykozidov pripravená na modernizáciu na priemyselnú úroveň a uprednostňujú sa chemické metódy.
V roku 1870 M.A. Colley oznámil syntézu „acetochlorhydrózy“ (1, obrázok 2) reakciou dextrózy (glukózy) s acetylchloridom, čo nakoniec viedlo k histórii syntézy glykozidov.
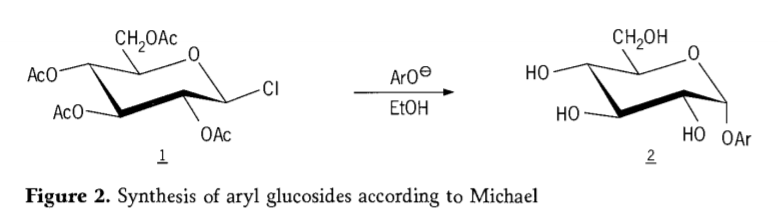
Tetra-0-acetyl-glukopyranosylhalogenidy (acetohaloglukózy) sa neskôr ukázali ako užitočné medziprodukty pre stereoselektívnu syntézu čistých alkylglukozidov. V roku 1879 sa Arthurovi Michaelovi podarilo pripraviť z Colleyho medziproduktov a fenolátov jednoznačné, kryštalizovateľné arylglykozidy (Aro-, obrázok 2).
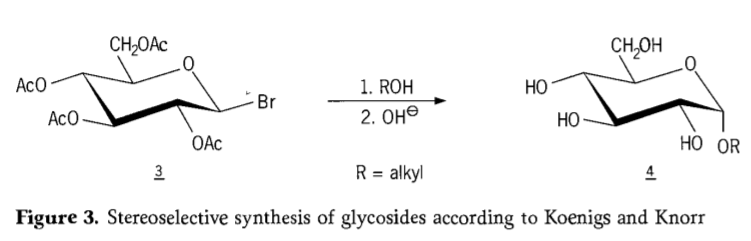
V roku 1901 Michaelova syntéza širokej škály sacharidov a hydroxylových aglykónov, keď W. Koenigs a E. Knorr predstavili svoj vylepšený stereoselektívny glykozidačný proces (obrázok 3). Reakcia zahŕňa substitúciu SN2 na anomérnom uhlíku a prebieha stereoselektívne s inverziou konfigurácie, pričom vzniká napríklad α-glukozid 4 z β-anoméru aceobromglukózového medziproduktu 3. Koenigsova-Knorrova syntéza prebieha v prítomnosti strieborných alebo ortuťových promótorov.
V roku 1893 navrhol Emil Fischer zásadne odlišný prístup k syntéze alkylglukozidov. Tento proces je dnes dobre známy ako „Fischerova glykozidácia“ a zahŕňa kyslo katalyzovanú reakciu glykóz s alkoholmi. Akýkoľvek historický záznam by však mal zahŕňať aj prvý zaznamenaný pokus A. Gautiera z roku 1874 o premenu dextrózy bezvodým etanolom v prítomnosti kyseliny chlorovodíkovej. Kvôli zavádzajúcej elementárnej analýze sa Gautier domnieval, že získal „diglukózu“. Fischer neskôr preukázal, že Gautierova „diglukóza“ bola v skutočnosti prevažne etylglukozid (obrázok 4).
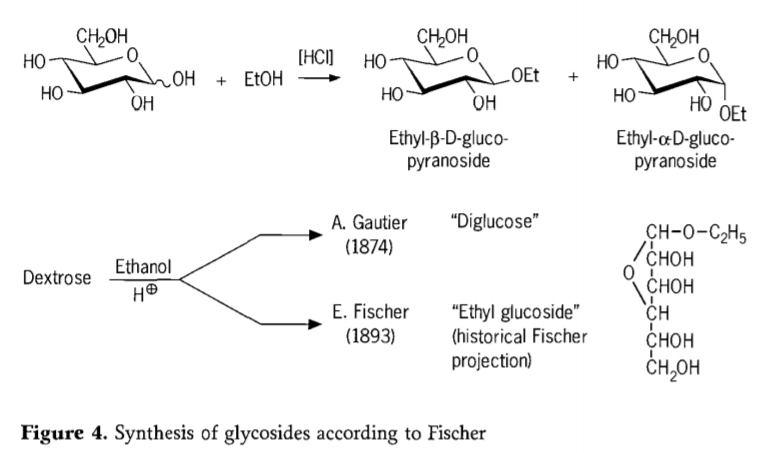
Fischer správne definoval štruktúru etylglukozidu, ako je zrejmé z navrhnutého historického furanozidového vzorca. V skutočnosti sú Fischerove glykozidačné produkty komplexné, väčšinou rovnovážne zmesi α/β-anomérov a izomérov pyranozid/furanozid, ktoré tiež obsahujú náhodne spojené glykozidové oligoméry.
Preto nie je ľahké izolovať jednotlivé molekulárne druhy z Fischerových reakčných zmesí, čo bol v minulosti vážny problém. Po určitom zlepšení tejto syntetickej metódy Fischer následne prijal pre svoje výskumy Koenigsovu-Knorrovu syntézu. Pomocou tohto postupu E. Fischer a B. Helferich ako prví v roku 1911 informovali o syntéze alkylglukozidu s dlhým reťazcom, ktorý vykazuje povrchovo aktívne vlastnosti.
Už v roku 1893 si Fischer správne všimol základné vlastnosti alkylglykozidov, ako je ich vysoká stabilita voči oxidácii a hydrolýze, najmä v silne alkalickom prostredí. Obe vlastnosti sú cenné pre alkylpolyglykozidy v aplikáciách povrchovo aktívnych látok.
Výskum súvisiaci s glykozidačnou reakciou stále prebieha a v poslednej dobe bolo vyvinutých niekoľko zaujímavých ciest ku glykozidom. Niektoré postupy syntézy glykozidov sú zhrnuté na obrázku 5.
Vo všeobecnosti možno chemické glykozidačné procesy rozdeliť na procesy vedúce ku komplexným oligomérnym rovnováham v kyselinou katalyzovanej glykozylovej výmene.
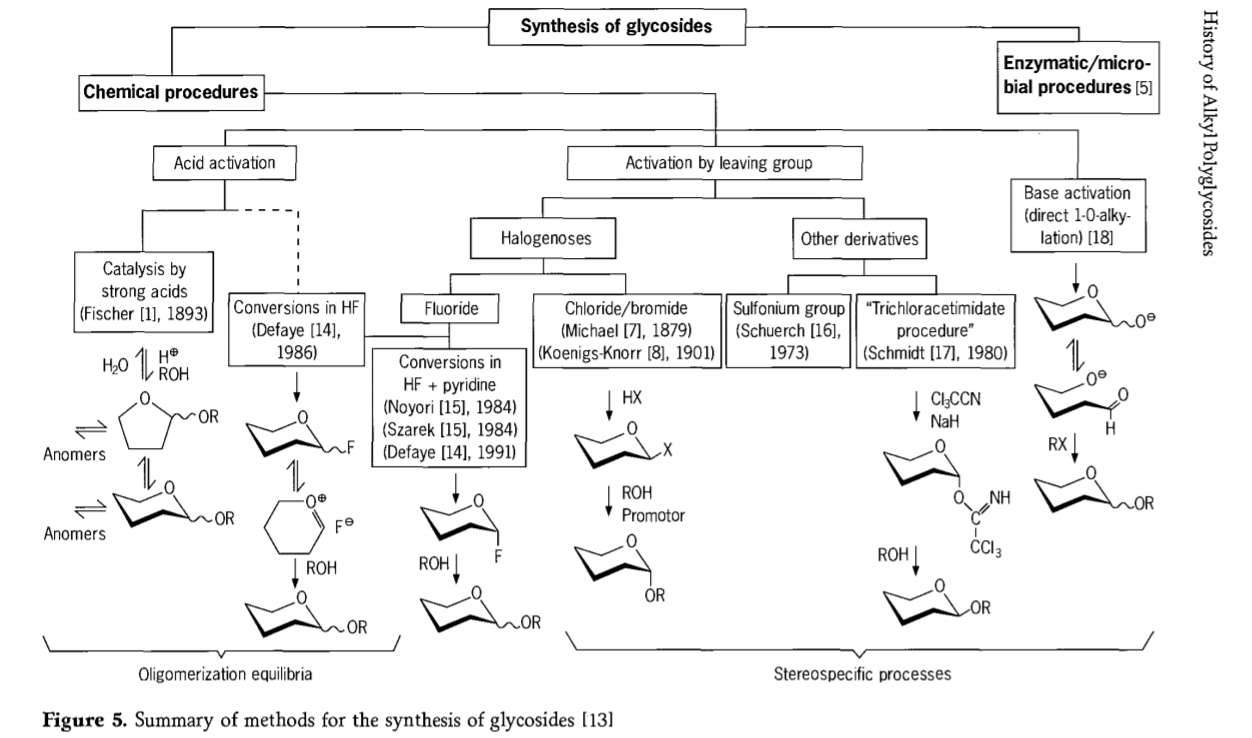
Reakcie na vhodne aktivovaných sacharidových substrátoch (Fischerove glykozidové reakcie a reakcie fluorovodíka (HF) s nechránenými molekulami sacharidov) a kineticky riadené, ireverzibilné a prevažne stereotaktické substitučné reakcie. Druhý typ postupu môže viesť k tvorbe jednotlivých druhov, a nie ku komplexným zmesiam reakcií, najmä v kombinácii s technikami konzervačných skupín. Sacharidy môžu zanechávať skupiny na ektopickom uhlíku, ako sú atómy halogénov, sulfonyly alebo trichlóracetimidátové skupiny, alebo môžu byť aktivované bázami pred premenou na triflátové estery.
V konkrétnom prípade glykozidácií vo fluorovodíku alebo v zmesiach fluorovodíka a pyridínu (pyridíniumpoly[fluorovodík]) sa glykozylfluoridy tvoria in situ a plynule sa premieňajú na glykozidy, napríklad s alkoholmi. Ukázalo sa, že fluorovodík je silne aktivačné, nedegradujúce reakčné médium; rovnovážna autokondenzácia (oligomerizácia) sa pozoruje podobne ako pri Fischerovom procese, hoci reakčný mechanizmus je pravdepodobne odlišný.
Chemicky čisté alkylglykozidy sú vhodné len na veľmi špeciálne aplikácie. Napríklad alkylglykozidy sa úspešne používajú v biochemickom výskume na kryštalizáciu membránových proteínov, ako je trojrozmerná kryštalizácia porínu a bakteriorodopsínu v prítomnosti oktyl β-D-glukopyranozidu (ďalšie experimenty založené na tejto práci viedli k Nobelovej cene za chémiu pre Deisenhofera, Hubera a Michela v roku 1988).
V priebehu vývoja alkylpolyglykozidov sa v laboratórnom meradle používali stereoselektívne metódy na syntézu rôznych modelových látok a na štúdium ich fyzikálno-chemických vlastností. Vzhľadom na ich komplexnosť, nestabilitu medziproduktov a množstvo a kritickú povahu odpadových produktov v procese by syntézy typu Koenigs-Knorr a iné techniky s ochrannými skupinami spôsobovali značné technické a ekonomické problémy. Procesy Fischerovho typu sú relatívne menej komplikované a ľahšie sa vykonávajú v komerčnom meradle, a preto sú preferovanou metódou na výrobu alkylpolyglykozidov vo veľkom meradle.
Čas uverejnenia: 12. septembra 2020





